目录
医疗器械留样的管理规程包含哪些内容?
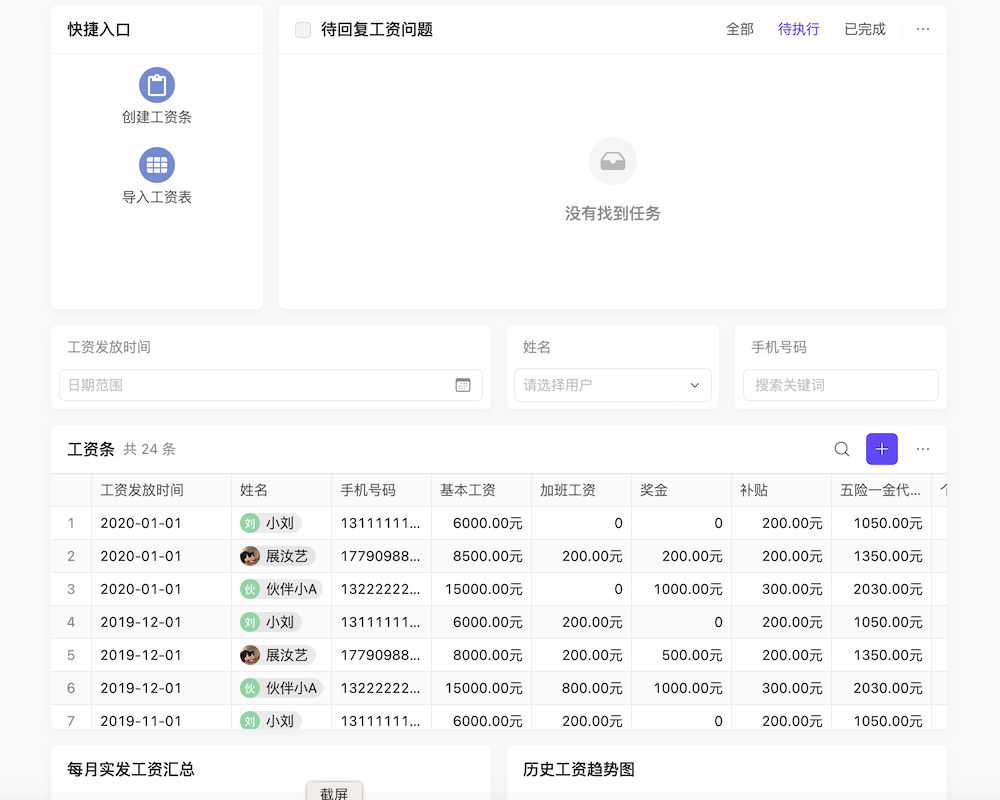
医疗器械生产和质量控制中,留样管理非常关键。其目的包括质量追溯、法规符合性和产品改进。留样范围按产品类型分有源、无源医疗器械和体外诊断试剂,按生产批次分首批生产和重大变更后的产品。数量方面既要满足法规最低要求,也要根据风险评估确定。保存条件上,不同器械对温湿度要求差异大,如体外诊断试剂、含橡胶部件器械、有源医疗器械等都有各自适宜的保存环境要求。
用户关注问题
医疗器械留样管理规程包括哪些方面?
就像我们公司刚涉足医疗器械这块,要做留样管理,但不知道从哪下手。这个管理规程到底都涵盖了哪些东西呢?是光把东西留着就行了吗?肯定不是这么简单吧,所以想了解下都包括啥方面。
医疗器械留样管理规程主要包括以下几个重要方面:
一、留样的范围确定
1. 首先要明确哪些医疗器械需要留样。一般来说,高风险的、新研发的、工艺复杂的医疗器械通常需要留样。例如植入式心脏起搏器这类高风险器械,必须留样以便后续追溯和调查。
二、留样数量与样本选取
1. 根据产品的生产批量、检验要求等来确定留样数量。如果是大批量生产的一次性注射器,要按照一定比例抽取足够数量的样本作为留样。
2. 在样本选取时,要确保具有代表性,可以采用随机抽样结合分层抽样的方法,保证不同批次、不同生产线的产品都能有留样。
三、留样的存储条件
1. 存储环境要符合医疗器械的特性。对于一些对温度、湿度敏感的试剂类医疗器械,要严格控制存储的温湿度范围,像某些酶类试剂可能需要低温冷藏保存。
2. 存储场所要有专人管理,防止样品被污染、损坏或者混淆。
四、留样的标识与记录
1. 每个留样都要有清晰的标识,标明产品名称、型号、规格、生产日期、批次等关键信息。这就好比给每个留样一个“身份证”,方便快速查找和识别。
2. 详细记录留样的入库时间、存储位置、检查情况等信息。这些记录在遇到质量问题追溯时非常关键。
如果您想要更深入地了解如何制定适合您企业的医疗器械留样管理规程,欢迎点击免费注册试用我们的专业咨询服务。

如何确保医疗器械留样管理规程的有效执行?
我们厂有了医疗器械留样管理规程,但是感觉执行起来老是不到位。比如说有时候员工会忘记检查留样,或者存储条件偶尔也没达标。怎么才能让这个规程有效地执行下去呢?就像盖房子有了图纸,但工人不按图施工可不行啊。
要确保医疗器械留样管理规程的有效执行,可以从以下几个要点入手:
一、人员培训
1. 对涉及到留样管理的工作人员进行全面培训,包括操作流程、质量意识等方面的培训。例如组织专门的课程,讲解留样的重要性以及操作不当可能带来的严重后果。
2. 定期考核员工对规程的掌握程度,只有考核通过的员工才能上岗操作。
二、监督与检查机制
1. 设立专门的监督岗位或者小组,定期检查留样管理工作。比如每周对留样存储环境进行一次检查,查看温湿度是否正常、样品有无损坏等。
2. 建立检查表,将每次检查的项目、结果详细记录下来。一旦发现问题,可以及时追踪责任人和整改情况。
三、信息化管理系统
1. 引入合适的信息化管理系统,将留样的所有信息录入系统。这样可以实现实时监控和提醒功能,例如当留样快到检查周期时,系统自动提醒相关人员。
2. 通过系统可以方便地查询历史数据和统计分析,有助于发现潜在的问题趋势。
如果您想进一步优化您企业的医疗器械留样管理规程执行情况,欢迎预约演示我们专门为此设计的管理工具。
医疗器械留样管理规程对企业质量管理有何意义?
我们企业在做质量管理,有人说医疗器械留样管理规程很重要,可是我不太明白它到底对质量管理有啥实际意义呢?感觉就是多留些产品放着而已,难道还有别的作用?就像是一堆零件放在仓库,不知道它们对整个机器运转有啥帮助一样。
医疗器械留样管理规程对企业质量管理有着多方面的重要意义:
一、质量追溯方面
1. 在出现产品质量问题时,留样能够提供最直接的证据。例如如果市场上反馈某批输液器存在漏液现象,企业可以通过对比留样,迅速查找出是生产环节、原材料还是其他方面的问题。这就像破案时的线索一样,帮助企业精准定位问题根源。
二、质量改进依据
1. 对留样进行定期的检测和分析,可以发现产品质量的变化趋势。比如通过对比不同批次的心脏支架留样的性能指标,若发现某项指标有下降趋势,企业就可以及时调整生产工艺或者原材料供应商,从而持续提升产品质量。
三、应对法规监管
1. 相关法规对医疗器械留样管理有明确要求,遵守规程有助于企业顺利通过监管部门的检查。否则可能面临处罚甚至产品召回等严重后果。这就如同遵守交通规则一样,是企业合法运营的必要条件。
如果您想提升企业质量管理水平,我们的专家团队可以为您提供更多关于医疗器械留样管理规程方面的指导,欢迎点击免费注册试用。
医疗器械留样管理规程中,留样期限如何确定?
我知道医疗器械要留样,但是这个留样留多久呢?总不能无限期地留着吧。是不是不同的器械留样期限不一样呢?就像食品有保质期一样,医疗器械的留样期限是不是也有个规定或者计算方法之类的呢?
在医疗器械留样管理规程中,留样期限的确定需要综合考虑多方面因素:
一、法规要求
1. 首先要遵循国家和地方相关法规的规定。有些地区对特定类型的医疗器械有明确的留样期限要求,如某些高风险的植入性医疗器械可能要求留样至产品有效期后若干年。
二、产品特性
1. 不同类型的医疗器械其稳定性、使用周期等特性不同。例如一次性医用口罩,由于其结构相对简单且使用周期短,留样期限可能相对较短;而大型的医疗设备,如磁共振成像设备,由于其结构复杂、使用寿命长且维修更换部件等情况较多,留样期限可能较长。
三、风险评估
1. 对产品的风险进行评估。高风险的医疗器械,如心脏起搏器,由于其一旦出现质量问题可能对患者生命健康造成严重威胁,留样期限往往较长,以确保在产品的整个生命周期内都能进行追溯和调查。
如果您想准确确定您企业生产的医疗器械的留样期限,欢迎预约演示我们的专业风险评估工具。
免责申明:本文内容通过 AI 工具匹配关键字智能整合而成,仅供参考,伙伴云不对内容的真实、准确、完整作任何形式的承诺。如有任何问题或意见,您可以通过联系 12345@huoban.com 进行反馈,伙伴云收到您的反馈后将及时处理并反馈。